Batería de Níquel-Cadmio: Funcionamiento y Características
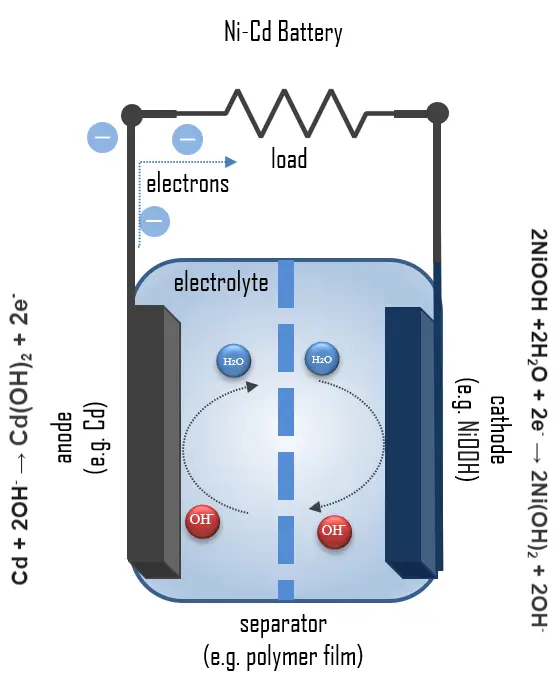
La batería de níquel-cadmio (batería Ni-Cd) es un tipo de batería secundaria que utiliza hidróxido de óxido de níquel Ni(O)(OH) como cátodo y cadmio metálico como ánodo. La abreviatura Ni-Cd proviene de los símbolos químicos del níquel (Ni) y el cadmio (Cd). Esta batería se caracteriza por tener una baja impedancia interna, lo que resulta en una alta capacidad de potencia, aunque su capacidad de almacenamiento de energía es menor en comparación con otros sistemas de baterías.
Una de las ventajas significativas de las baterías Ni-Cd es su larga vida útil y la capacidad de recarga rápida. Sin embargo, pueden sufrir de depresión de voltaje o efecto memoria, lo que significa que el voltaje de carga máximo disminuirá, así como la capacidad energética, si se descargan continuamente de manera superficial. Su mayor desventaja es el contenido de cadmio, un metal extremadamente tóxico, lo que descarta a las baterías Ni-Cd como una alternativa moderna para sistemas de baterías.
Aplicaciones de la Batería de Níquel-Cadmio
Actualmente, las aplicaciones de las baterías de níquel-cadmio se encuentran en dispositivos portátiles de pequeño tamaño, como herramientas eléctricas, juguetes, iluminación de emergencia, instrumentación médica o productos industriales portátiles. Se utilizan en productos de pequeño tamaño ya que su costo para aplicaciones de baja potencia es económico, pero son tres a cuatro veces más caras que las baterías de plomo-ácido para la misma capacidad.
Química de la Batería de Níquel-Cadmio
Una celda Ni-Cd completamente cargada contiene:
- Cátodo: una placa de electrodo positivo de óxido-hidróxido de níquel(III).
- Ánodo: una placa de electrodo negativo de cadmio.
- Separador.
- Electrolito: un electrolito alcalino (hidróxido de potasio).
Las baterías Ni-Cd suelen tener una carcasa metálica con una placa de sellado equipada con una válvula de seguridad auto sellante. Las placas de electrodos positivos y negativos, aisladas entre sí por el separador, están enrolladas en forma espiral dentro de la carcasa. Este diseño, conocido como «jelly-roll», permite que una celda Ni-Cd entregue una corriente máxima mucho más alta que una celda alcalina de tamaño equivalente.
El electrodo positivo en el estado de descarga está compuesto por hidróxido de níquel, que ha sido dopado y modificado para cumplir con los requisitos de la batería, y grafito como medio conductor. El níquel alterna entre dos estados de oxidación durante la carga y descarga; al cargar, el hidróxido de níquel se convierte en oxihidróxido de níquel (NiOOH):
2Ni(OH)2 + 2OH– → 2NiOOH + 2H2O + 2e–
Durante la descarga, las reacciones en el electrodo de óxido de níquel son:
2NiOOH + 2H2O + 2e– → 2Ni(OH)2 + 2OH–
El electrodo negativo consiste en hidróxido de cadmio, Cd(OH)2, que se reduce a cadmio metálico durante la carga. La reacción se invierte durante el proceso de descarga, cambiando el estado de oxidación del cadmio de 0 a 2+, liberando dos electrones por cada átomo de cadmio que participa en la reacción. A continuación, se muestra la reacción para el ánodo durante la carga:
Cd(OH)2 + 2e– → Cd + 2OH–
Las reacciones químicas en el electrodo de cadmio durante la descarga son:
Cd + 2OH– → Cd(OH)2 + 2e–
La reacción general durante la descarga es:
2NiOOH + Cd + 2H2O → 2Ni(OH)2 + Cd(OH)2
El cadmio es un metal bastante peligroso por sí solo, por lo tanto, existen una serie de regulaciones y pautas sobre cómo manejarlo establecidas por gobiernos de todo el mundo y la UE. El electrolito actúa como portador de carga de iones en las baterías, y para las baterías Ni-Cd, esto consiste principalmente en hidróxido de potasio concentrado, KOH, pero también puede tener adiciones de hidróxido de sodio, NaOH, y hidróxido de litio, LiOH.